2019年廣東省深圳市中考化學試卷
一、選擇題(共10小題,每小題1.5分,共15分.在每小題給出的4個選項中,只有一項符合題意.)
1.(1.5分)化學與人類的生產、生活密切相關。下列描述正確的是( )
A.引起貧血的主要原因是缺鋅B.不合理施用化肥會造成水體污染
C. 是電池回收標志D.用水噴淋燃著的酒精以降低著火點
是電池回收標志D.用水噴淋燃著的酒精以降低著火點
2.(1.5分)下列化學用語表述正確的是( )
A.硫酸鉀的化學式:K2SO4B.1個氯分子:Cl
C.2個硝酸根:2NO2D.銅離子:![]()
3.(1.5分)下列實驗不涉及化學變化的是( )
|
|
|
|
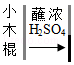
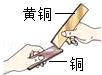
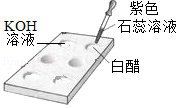
測定空氣中O2的含量 | 驗證濃H2SO4的腐蝕性 | 比較合金與純金屬的硬度 | 判斷溶液的酸堿性 |
A.AB.BC.CD.D
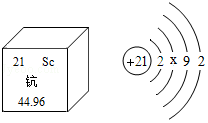
4.(1.5分)鈧(Kc)是一種“工業的維生素”。圖為鈧在元素周期表中的相關信息及其原子的結構示意圖。下列說法正確的是( )
A.鈧屬于非金屬元素
B.鈧的相對原子質量是21
C.原子結構示意圖中x=10
D.鈧原子核外有四個電子層
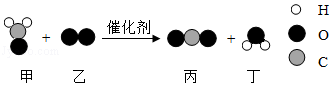
5.(1.5分)科學家研制出一種新型催化劑,可用于去除裝修殘留的甲醛(化學式為CH2O),該反應過程的微觀示意圖如圖。下列說法正確的是( )
A.物質甲為甲醛,其分子由碳原子和水分子構成B.物質乙中氧元素的化合價為﹣2價
C.該反應前后原子種類和數目均發生改變D.該反應消耗物質甲和生成物質丁的質量比為5:3
6.(1.5分)CuO粉末與H2在加熱條件下會發生反應。下列說法錯誤的是( )
A.反應所需H2可由Cu與稀H2SO4反應制得B.反應過程可觀察到固體粉末由黑色變成紅色
C.發生的反應為CuO+H2![]() Cu+H2OD.該反應說明H2具有還原性
Cu+H2OD.該反應說明H2具有還原性
7.(1.5分)異煙肼(化學式:C6H7N3O;相對分子質量:137)是治療肺結核藥物的有效成分。下列說法正確的是( )
A.異煙肼屬于氧化物B.異煙肼分子中H、O原子個數比為7:1
C.異煙肼中C、H兩種元素的質量比為36:7
D.異煙肼中N元素質量分數的計算式為![]() ×100%
×100%
8.(1.5分)為達到以下實驗目的,下列相應實驗方案合理的是( )
選項 | 實驗目的 | 實驗方案 |
A | 獲得廉價的新能源 | 電解水制H2 |
B | 將河水凈化為純水 | 經沉淀、過濾、吸附 |
C | 驗證金屬活動性Zn>Cu | 利用Zn片與CuSO4溶液的反應 |
D | 除去NaCl固體中少量的MgCl2 | 加水溶解,再加入過量NaOH溶液 |
A.AB.BC.CD.D
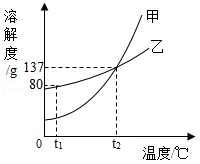 9.(1.5分)現有t2℃時的溶液Ⅰ、Ⅱ各100g,溶液I中含物質甲50g,
9.(1.5分)現有t2℃時的溶液Ⅰ、Ⅱ各100g,溶液I中含物質甲50g,
溶液Ⅱ是物質乙的飽和溶液。物質甲、乙(均不含結晶水)的溶解度
曲線如圖所示。下列說法正確的是( )
A.t2℃時,溶液Ⅰ是甲的飽和溶液
B.t2℃時,溶液Ⅰ中甲的質量分數為50%
C.t2℃時,溶液Ⅱ中含乙37g
D.從t2℃降溫至t1℃時,乙不會從溶液Ⅱ中析出
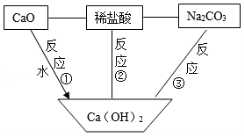 10.(1.5分)關系圖中“﹣”兩端的物質能發生化學反應,“→”表示物質的轉化方向。下列說法錯誤的是( )
10.(1.5分)關系圖中“﹣”兩端的物質能發生化學反應,“→”表示物質的轉化方向。下列說法錯誤的是( )
A.反應①放出熱量
B.反應②所得溶液可呈中性
C.反應③可得NaOH
D.不能將圖中稀鹽酸換為稀H2SO4
二、非選擇題(共3題,共25分)
11.(8分)生鐵用途十分廣泛。工業上利用赤鐵礦(主要成分是Fe2O3,還含少量SiO2等雜質)冶煉生鐵的過程如圖:

回答下列問題:
(1)生鐵屬于材料(填“合成”或“金屬”)。“高爐氣體”中的(填化學式)會導致酸雨。
(2)“煅燒”時:
①生成CO的反應之一為C+CO2![]() 2CO,該反應屬于反應(填基本反應類型)。
2CO,該反應屬于反應(填基本反應類型)。
②用化學方程式表示利用CO煉鐵的原理。
③CaCO3和SiO2固體在高溫條件下發生反應,生成CO2氣體和CaSiO3,該反應的化學方程式為。
(3)生活中鐵制品銹蝕的過程,實際上是Fe與空氣中、等發生化學反應的過程。下列措施能防止鐵制品銹蝕的是(填標號)。
A.涂油、噴漆B.鍍耐腐蝕的鉻層C.用鹽水清洗D.久置于酸性環境
12.(8分)為探究某塑料的組成元素,設計了實驗I和II.回答下列問題:
I.制取氧氣
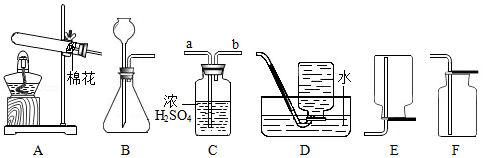
(1)若用一種暗紫色固體制取O2,發生反應的化學方程式為,發生裝置應選擇上述裝置(填標號)。
(2)欲制取干燥的O2,裝置合理的連接順序為:發生裝置→C→(填標號)。連接裝置時,發生裝置的出氣口應與裝置C中(填“a”或“b”)端相連。
II.組成探究
(3)定性檢測(已知:無水CuSO4遇水變藍色)
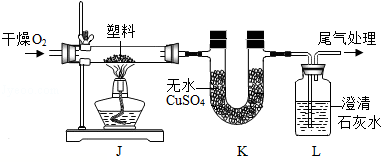
實驗操作 | 實驗現象 | 結論 |
連接裝置,檢查氣密性,裝入試 劑并按如圖進行實驗。通入O2, 一段時間后,點燃J處酒精燈。 | 裝置K中無水CuSO4變 ①色 | 塑料燃燒產物中有H2O |
裝置L中②。 | 塑料燃燒產物中有CO2 |
③由上述實驗可知,該塑料一定含有的元素是(填元素符號)。
(4)定量測定
為進一步確定組成,將1.4g該塑料在足量O2中完全燃燒,共產生了4.4g CO2和1.8g H2O,依據質量守恒定律,可判斷該塑料(填“含有”或“不含”)除上述③中結論之外的元素。
13.(9分)已知:①NaHCO3固體受熱分解2NaHCO3![]() Na2CO3+CO2↑+H2O;②Na2CO3受熱不分解。回答下列問題:
Na2CO3+CO2↑+H2O;②Na2CO3受熱不分解。回答下列問題:
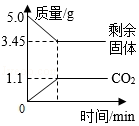
(1)關于NaHCO3固體的敘述錯誤的是(填標號)。欲測定某NaHCO3固體樣品(只含Na2CO3雜質且分布均勻)中NaHCO3的質量分數,將5.0g該樣品加熱至質量不再改變,測得剩余固體的質量、生成CO2的質量隨時間變化如圖所示。
A.俗稱小蘇打B.難溶于水
C.可與稀鹽酸發生反應D.是發酵粉的主要成分之一
(2)欲測定某NaHCO3固體樣品(只含Na2CO3雜質且分布均勻)中NaHCO3的質量分數,將5.0g該樣品加熱至質量不再改變,測得剩余固體的質量、生成CO2的質量隨時間變化如圖所示。
①NaOH溶液的pH7(填“>”、“=”或“<”),用該溶液將生成的CO2完全吸收,發生反應的化學方程式為。
②由圖中數據可知,上述5.0g NaHCO3樣品完全分解產生CO2的質量為g,產生H2O的質量是g。
③計算該樣品中NaHCO3的質量分數(根據化學方程式寫出完整的計算步驟)。